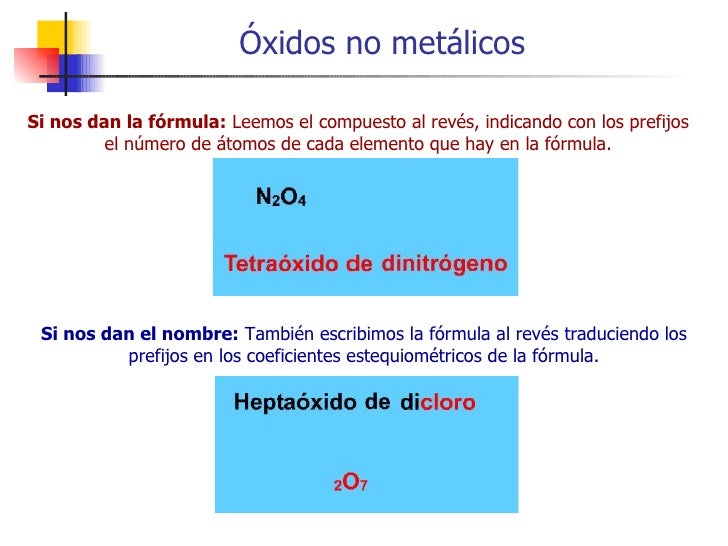
Los óxidos no metálicos son compuestos moleculares binarios resultantes de la combinación de un elemento no metálico con el oxígeno. También pueden ser llamados óxidos ácidos. Su fórmula puede ser expresada como: X2On, dónde: X, representa el elemento metálico. N, representa la valencia de dicho metal.. mono- di- tri- tetra- penta- hexa- hepta- octa- nona- deca- undeca- dodeca-. Ejemplos de óxidos no metálicos: N 2 O Óxido de dinitrógeno. NO Monóxido de nitrógeno. N 2 O 3 Trióxido de dinitrógeno. N 2 O 4 Tetraóxido de dinitrógeno. CO Monóxido de carbono. CO 2 Dióxido de carbono. Cl 2 O 7 Heptaóxido de dicloro.

Nomenclatura de óxidos no metálicos │química YouTube

Usos Y Aplicaciones De Los Oxidos No Metalicos Aplican Compartida
Oxidos No MetáLicos

Oxidos No Metalicos Nomenclatura Tados

Óxidos Metálicos No Metálicos y Peróxidos Deyleen Mejía Rengifo uDocz

lectura 1, ¿EN QUÉ DIFEREN LOS ÓXIDOS METÁLICOS DE LOS NO METÁLICOS?,…

CÓMO SE HACEN LOS ÓXIDOS BÁSICOS YouTube

Como Se Forman Los Oxidos No Metalicos buick

Óxidos No Metálicos (Anhídridos) YouTube

óXidos acidos o no metálicos

Quimica1 Caracteristicas de los oxidos no metalicos.
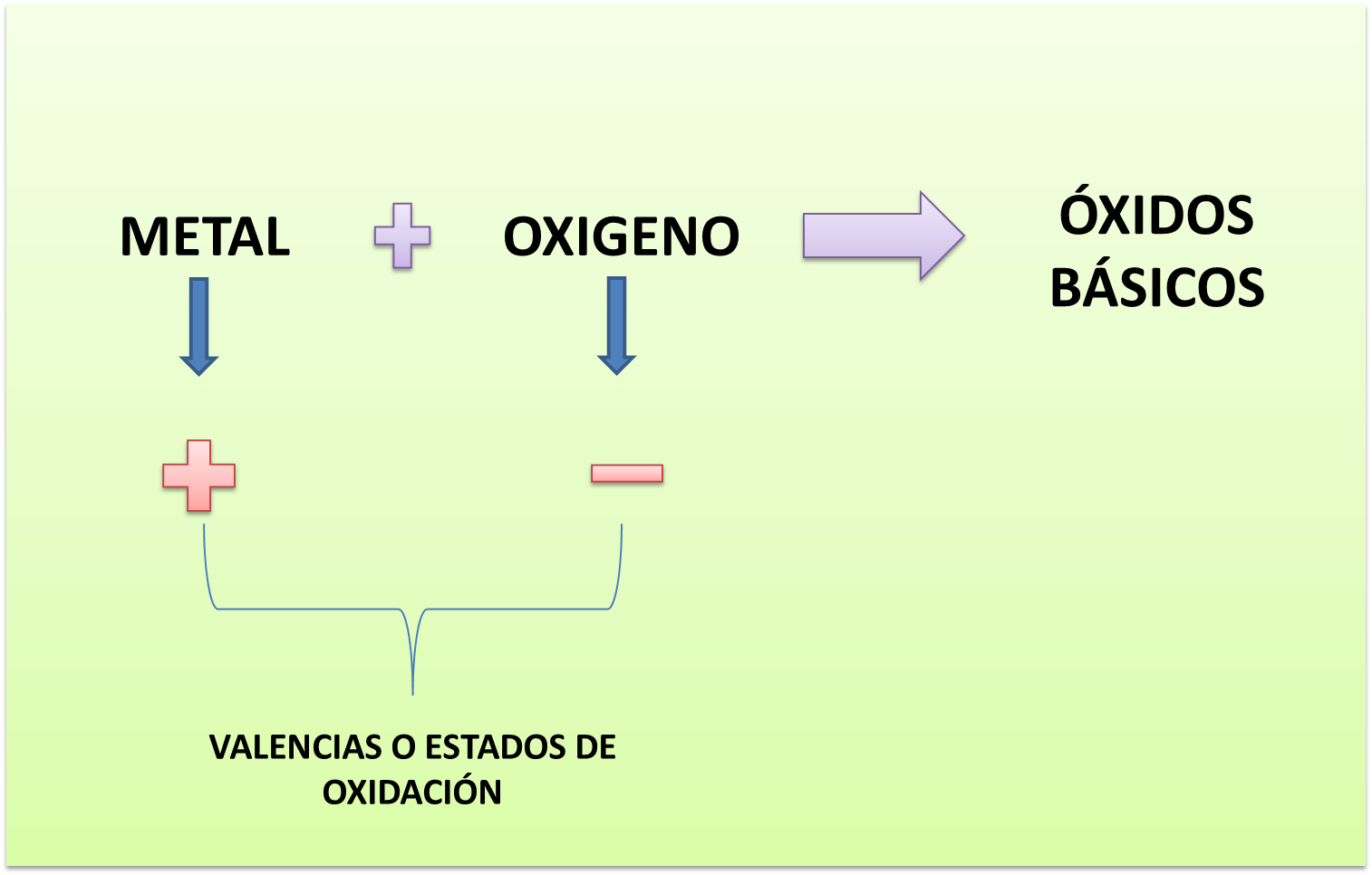
ÓXIDOS BÁSICOS // Formulación y nomenclatura. — Hive
FORMACIÓN Y NOMENCLATURA DE ÓXIDOS NEUTROS YouTube

Usos Y Aplicaciones De Los Oxidos No Metalicos Aplican Compartida
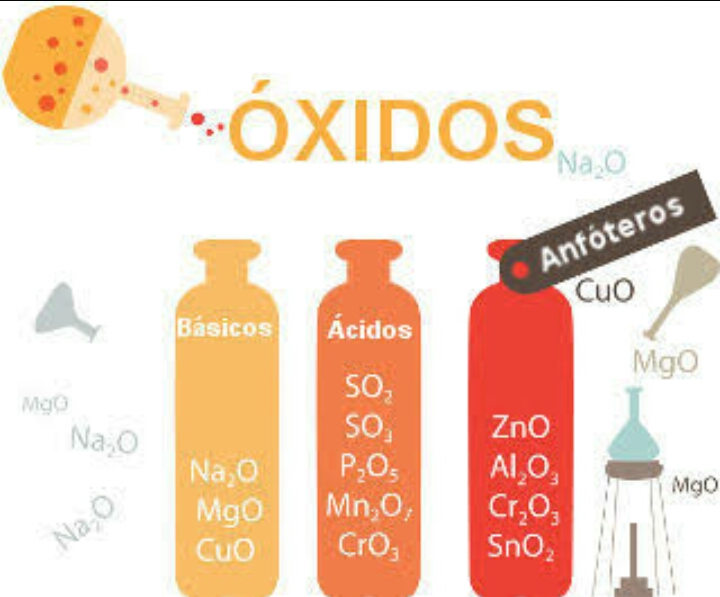
EL BLOG DEL QUIMICO... Óxidos básicos y su nomenclatura

USOS DE OXIDOS NO METALICOS YouTube

Oxidos No Metalicos Nomenclatura Tados

Como Se Forma Un Oxido No Metalico buick

Quimica Caracteristicas de los Metales, No metales y Metaloides

Formulación de Óxidos No Metálicos (con Halógenos) YouTube
Óxidos No Metálicos y su Uso Cotidiano. DEFINICIÓN: Los óxidos no metálicos son compuestos de tipo binario, que se forman a partir de la combinación entre un no metal y el oxígeno. Estos conjuntos de compuestos son también llamados óxidos ácidos o anhídridos. FÓRMULA: La forma de los anhídridos u óxidos no metálicos es del tipo.. Propiedades de los óxidos no metálicos. Son compuestos de bajos puntos de fusión, formados al reaccionar un no metal con el oxígeno. Se pueden encontrar en diferentes estados de la materia. Forman ácidos al combinarse con el agua. Presentan altos números de oxidación. En la tabla periódica, su carácter ácido se incrementa de izquierda.